Onderzoek van de Universiteit van Osaka benadrukt de cruciale rol van het HKDC1-eiwit bij het in stand houden van de mitochondriën en lysosomen, waardoor celveroudering en aanverwante ziekten worden voorkomen. Deze ontdekking opent nieuwe potentiële therapeutische benaderingen voor verouderingsgerelateerde aandoeningen. Krediet: SciTechDaily.com
Onderzoekers van de Universiteit van Osaka hebben een eiwit geïdentificeerd, HKDC1 genaamd, dat essentieel is voor het in stand houden van twee cellulaire structuren, de mitochondriën en de lysosomen, en zo cellulaire veroudering voorkomt.
Net zoals gezonde organen essentieel zijn voor ons welzijn, zijn gezonde organellen essentieel voor een goede celfunctie. Deze subcellulaire structuren vervullen specifieke functies binnen de cel. Mitochondriën voorzien de cel bijvoorbeeld van energie en lysosomen houden de cel netjes.
Een doorbraak in het begrijpen van het onderhoud van organellen
Hoewel schade aan deze twee organellen in verband wordt gebracht met veroudering, cellulaire veroudering en vele ziekten, is de regulering en het onderhoud van deze organellen nog steeds slecht begrepen. Nu hebben onderzoekers van de Universiteit van Osaka een eiwit geïdentificeerd, HKDC1, dat een sleutelrol speelt bij het in stand houden van deze twee organellen en zo celveroudering helpt voorkomen.
Er zijn aanwijzingen dat een eiwit genaamd TFEB betrokken is bij het in stand houden van de functie van beide organellen, maar er zijn geen doelwitten voor dit eiwit geïdentificeerd. Door alle genen van een cel te vergelijken die onder bepaalde omstandigheden actief zijn, en door gebruik te maken van een methode genaamd chromatine-immunoprecipitatie, die DNA Tegenover de eiwitten was het team de eerste die aantoonde dat het gen dat codeert voor HKDC1 een direct doelwit is van TFEB, en dat HKDC1 opgereguleerd wordt onder omstandigheden van mitochondriale of lysosomale stress.
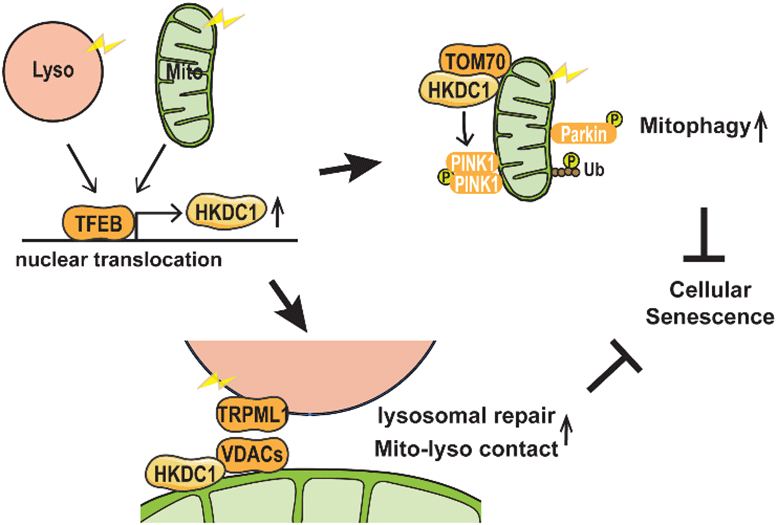
Overzicht: Zowel mitochondriale als lysosomale stress induceren nucleaire translocatie van TFEB, gevolgd door verhoogde HKDC1-expressie. HKDC1 stabiliseert PINK1 door interactie met TOM70, waardoor PINK1/Parkine-afhankelijke mitofagie wordt vergemakkelijkt. Bovendien zijn de HKDC1- en VDAC-eiwitten waarmee het interageert belangrijk voor het repareren van beschadigde lysosomen en voor het in stand houden van de communicatie tussen mitochondriën en lysosoom. HKDC1 voorkomt door DNA-schade geïnduceerde cellulaire veroudering door de mitochondriale en lysosomale homeostase te behouden. Bron afbeelding: 2024 Cui et al., HKDC1, een doelwit van TFEB, is essentieel voor het handhaven van de mitochondriale en lysosomale homeostase en het voorkomen van cellulaire veroudering. Met mensen
Mitochondriale beschermingsmechanismen
Eén manier om mitochondriën tegen schade te beschermen is door het proces van mitofagie, wat de gecontroleerde verwijdering van beschadigde mitochondriën is. Er zijn verschillende mitofagieroutes, waarvan de meest gekarakteriseerde afhankelijk zijn van eiwitten genaamd PINK1 en Parkin.
“We hebben waargenomen dat HKDC1 co-lokaliseert met een eiwit genaamd TOM20, dat zich in het buitenste mitochondriale membraan bevindt”, legt hoofdauteur Mengying Cui uit, “en door onze experimenten ontdekten we dat HKDC1, en de interactie ervan met TOM20, van cruciaal belang is voor verzwakking van PINK1/Parkine-afhankelijke mitofagie.”
Rol van HKDC1 bij lysosomaal herstel
Simpel gezegd: HKDC1 wordt door TFEB binnengebracht om mitochondriaal afval te helpen verwijderen. Maar hoe zit het met lysosomen? Welnu, TFEB en KHDC1 zijn hier ook grote spelers. Er is aangetoond dat het verminderen van HKDC1 in de cel het lysosomale herstel verstoort, wat suggereert dat HKDC1 en TFEB lysosomen helpen herstellen van schade.
‘HKDC1 is toch gelokaliseerd in de mitochondriën?’ ‘Dit lijkt ook cruciaal te zijn voor het lysosomale herstelproces’, legt hoofdonderzoeker Shuhei Nakamura uit. ‘Lysosomen en mitochondriën communiceren met elkaar via eiwitten die VDAC’s worden genoemd. Concreet is HKDC1 verantwoordelijk voor de interactie met VDAC's; Dit eiwit is essentieel voor de communicatie tussen mitochondriën en lysosomen, en dus voor lysosomaal herstel.
Potentiële therapeutische effecten
Deze twee verschillende functies van HKDC1, met een sleutelrol in zowel het lysosoom als de mitochondriën, helpen cellulaire veroudering te voorkomen door tegelijkertijd de stabiliteit van deze twee organellen te behouden. Omdat disfunctie van deze organellen geassocieerd is met veroudering en leeftijdsgebonden ziekten, opent deze ontdekking nieuwe horizonten voor therapeutische benaderingen voor deze ziekten.
Referentie: “HKDC1, een doelwit van TFEB, is essentieel voor het handhaven van de mitochondriale en lysosomale homeostase en het voorkomen van cellulaire veroudering” Met mensen.
doi: 10.1073/pnas.2306454120
Financiering: Japan Society for the Promotion of Science, Japan Science and Technology Agency, Ministerie van Onderwijs, Cultuur, Sport, Wetenschap en Technologie, Japan Medical Research and Development Agency
